El módulo de Química en el EXANI-II evalúa los conocimientos fundamentales que todo aspirante debe dominar para carreras de ciencias, ingenierías y áreas de la salud. Este simulador reproduce las condiciones del examen real, ayudándote a familiarizarte con el tipo de reactivos, la manera en que se formulan y la presión del tiempo.
Las preguntas están clasificadas por tema, de manera que puedas identificar a qué área corresponde cada una y enfocar tu estudio de forma precisa. Algunos temas estarán disponibles de manera gratuita para que comiences a practicar sin costo, pero si quieres acceder a todas las explicaciones detalladas y al material completo, podrás hacerlo al desbloquear el curso en Pasatuexam.
¿Qué mide este simulador?
El simulador de Química mide tu dominio en:
- Fundamentos generales: enlaces químicos, electronegatividad y tipos de enlace.
- Soluciones y concentraciones: ppm, molaridad y diferencias entre soluciones diluidas y concentradas.
- Balanceo de ecuaciones químicas: ajuste de coeficientes y descomposición térmica.
- Estequiometría: relaciones molares, masa y volumen de reactivos y productos.
- Reacciones químicas: neutralización, combustión y procesos endotérmicos y exotérmicos.
- Química orgánica: hibridación del carbono, nomenclatura de hidrocarburos y grupos funcionales.
- Biomoléculas: enlaces glicosídicos y peptídicos en proteínas y carbohidratos.
Estos conocimientos no solo son clave para tu examen, sino también para tu formación universitaria en áreas como medicina, biología, ingeniería química y más.
SIMULADOR DE QUÍMICA
Fundamentos generales: Enlaces químicos y su relación con la electronegatividad
1. Identifique el compuesto que presenta un enlace iónico.
- O2
- NaCl
- CO
Explicación:
Respuesta correcta b) NaCl.
El compuesto NaCl, o cloruro de sodio, exhibe un enlace iónico característico debido a la significativa diferencia de electronegatividad entre el sodio (Na) y el cloro (Cl), que es aproximadamente de 2.1. Esta gran diferencia facilita la transferencia completa de electrones del metal (Na) al no metal (Cl), resultando en la formación de iones Na+ y Cl− que se atraen electrostáticamente.
Las otras opciones no son respuestas correctas por las siguientes razones:
- a) O2 es incorrecto porque está formado por dos átomos del mismo elemento, oxígeno, que comparten electrones de manera equitativa, lo que resulta en un enlace covalente no polar. No hay diferencia de electronegatividad entre los mismos átomos.
- c) CO es incorrecto ya que es una molécula con un enlace covalente polar entre carbono (C) y oxígeno (O). Aunque hay una diferencia de electronegatividad entre C y O, los electrones son compartidos y no hay una transferencia completa como en los enlaces iónicos.
2. Si la diferencia de electronegatividad entre el Ca y O es de 2.5, ¿qué tipo de enlace los une para formar un compuesto?
- Covalente
- Iónico
- Metálico
Explicación:
Respuesta correcta b) Iónico.
El enlace entre el calcio (Ca) y el oxígeno (O) es iónico debido a la diferencia de electronegatividad de 2.5, que supera el umbral generalmente aceptado de 1.7 para la formación de enlaces iónicos. En este caso, el Ca, con una electronegatividad de aproximadamente 1.0, cede electrones al O, que tiene una electronegatividad de alrededor de 3.5, formando iones Ca2+ y O2− que se unen electrostáticamente.
Las otras opciones no son respuestas correctas por las siguientes razones:
- a) Covalente es incorrecto porque aunque el oxígeno y el calcio podrían compartir electrones, la gran diferencia de electronegatividad favorece la transferencia completa de electrones y la formación de un enlace iónico.
- c) Metálico es incorrecto ya que los enlaces metálicos se forman entre átomos de metales, y el oxígeno no es un metal.
Fundamentos generales: Soluciones (Tipos, porcentaje, partes por millón y molaridad de soluciones)
3. ¿Cuál es la cantidad en partes por millón de 2.25 mg de sulfatos (SO4) presentes en una muestra de 350 mL de agua?
- 0.006 ppm
- 0.064 ppm
- 6.428 ppm
Explicación:

4. ¿Cuál de las siguientes sustancias corresponde a una solución diluida?
- Néctar de frutas
- Agua de sabor
- Aderezo para ensalada
Explicación:
Respuesta correcta a) Agua de sabor.
El agua de sabor generalmente contiene una cantidad relativamente baja de soluto (azúcares, esencias o colorantes) en comparación con el solvente (agua), lo que la convierte en una solución diluida.
Las otras opciones no son correctas porque:
- El néctar de frutas y el aderezo para ensalada suelen tener concentraciones más altas de solutos como azúcares, aceites y otros ingredientes, lo que las hace más concentradas en comparación con las aguas de sabor.
5. Se pesó 1 g de NaOH y se disolvió en 100 mL de agua. ¿Cuál es la concentración molar de la disolución resultante, considerando que la masa del NaOH es de 40 g/mol?
- 0.00025 M
- 0.25 M
- 0.40 M
Explicación:

Fundamentos generales: Balanceo de ecuaciones químicas
6. Un químico calienta en un crisol carbonato de plata a temperaturas superiores a 1 000 °C; se producen óxido de plata y dióxido de carbono.
Identifique la ecuación que representa el proceso descrito.
Ag₂CO₃ → Ag₂O + CO₂
AgCO₃ → Ag₂O + CO₂
Ag₂CO₃ → AgO + CO₂
Explicación:
Respuesta correcta: c) Ag₂CO₃ → AgO + CO₂
Respuesta correcta a) Ag₂CO₃ → Ag₂O + CO₂.
Esta es la ecuación que correctamente representa la descomposición térmica del carbonato de plata (Ag₂CO₃). Al calentar este compuesto, se descompone en óxido de plata (Ag₂O) y dióxido de carbono (CO₂), manteniendo los números de oxidación de todos los elementos según lo establecido en la tabla periódica. El óxido de plata contiene dos átomos de plata, como en el reactivo original, y se produce una molécula de dióxido de carbono.
La opción b) AgCO₃ → Ag₂O + CO₂ no es correcta porque AgCO₃ sugiere un compuesto que no existe con un solo átomo de plata, lo cual es incorrecto ya que el carbonato de plata tiene la fórmula Ag₂CO₃, con dos átomos de plata.
La opción c) Ag₂CO₃ → AgO + CO₂ tampoco es correcta porque AgO implicaría un óxido con una proporción de 1:1 de plata a oxígeno, lo cual no es consistente con los productos de la descomposición del carbonato de plata.
7. Identifique los coeficientes que balancean la ecuación.
__H₂SO4+__NaHC₃→__Na₂SO4+__CO₂+__H₂O
- 1, 1, 1, 2, 1
- 1, 2, 1, 2, 2
- 2, 1, 2, 1, 2
Ojo: el simulador del EXANI-II tiene un error aquí, la ecuacion correcta a balancear es:
__H₂SO₄+__NaHCO₃→__Na₂SO₄+__CO₂+__H₂O
Ten en cuenta que se pueden equivocar al plantear las preguntas en tu EXANI-II, aun asi busca encontrar la respuesta correcta.
Explicación:
Respuesta correcta: b) 1, 2, 1, 2, 2
Ecuación a balancear:
__H2SO₄ + __NaHCO₃ → __Na2SO₄ + __CO₂ + __H₂O
Pasos para el Balanceo:
- Balanceo del sodio (Na): Tenemos 1 átomo de sodio en el bicarbonato de sodio (NaHCO₃) y necesitamos 2 para el sulfato de sodio (Na₂SO₄). Ajustamos la ecuación para el sodio añadiendo un coeficiente de 2 frente al NaHCO₃:
__H2SO₄ + 2NaHCO₃ → __Na2SO₄ + __CO2 + __H2O
- Balanceo del carbono (C): Con el ajuste previo, ahora tenemos 2 átomos de carbono del bicarbonato de sodio. Necesitamos dos moléculas de CO₂ para balancear los átomos de carbono:
__H2SO₄ + 2NaHCO₃ → __Na₂SO₄ + 2CO₂ + __H₂O
- Balanceo del oxígeno (O): Después de balancear el carbono, contamos los átomos de oxígeno. En el reactivo, tenemos 4 oxígenos del H₂SO₄ y 3 oxígenos de cada NaHCO₃, sumando un total de 10 oxígenos. En el producto, tenemos 4 oxígenos en el Na₂SO₄ y 2 oxígenos en cada CO₂, sumando un total de 8 oxígenos, más los oxígenos del agua que aún no hemos balanceado. Para igualar los oxígenos, ajustamos la cantidad de moléculas de agua a 2, sumando un total de 10 oxígenos en el lado del producto:
__H₂SO₄ + 2NaHCO₃ → __Na₂SO₄ + 2CO2 + 2H₂O
- Balanceo del hidrógeno (H): Ahora consideramos los hidrógenos. En los reactivos, tenemos 2 hidrógenos del H₂SO₄ y 2 más de los 2 NaHCO₃ (1 por cada uno), lo que nos da un total de 4 hidrógenos. Para equilibrar los hidrógenos en los productos, necesitamos 2 moléculas de H₂O, ya que cada una aporta 2 hidrógenos, en este caso los hidrogenos estan balanceados en ambos lados.
__H₂SO₄ + 2NaHCO₃ → __Na₂SO₄ + 2CO₂ + 2H₂O
Ecuación balanceada:
1H₂SO₄ + 2NaHCO₃ → 1Na₂SO₄ + 2CO₂ + 2H₂O
8. En el compuesto 3Ca2(PO4)2 hay ___ átomos de _______.
- 3, calcio
- 6, fósforo
- 8, oxígeno
Explicación:
Respuesta correcta a) 6, fósforo.
En el compuesto 3Ca₂ (PO₄)₂, primero se observa el coeficiente global de 3, que multiplica a todos los átomos dentro del compuesto. El grupo (PO₄) tiene un subíndice de 2, lo que indica que hay dos grupos de fosfato en la fórmula unitaria. Sin embargo, cada grupo fosfato contiene solo un átomo de fósforo (P). Por lo tanto, para contar el total de átomos de fósforo, se multiplican los átomos de fósforo en un grupo fosfato (1) por el número de grupos fosfato (2) y luego por el coeficiente global (3): 1 (P) * 2 (PO₄) * 3 = 6 átomos de fósforo.
Explicación de por qué las otras respuestas no son correctas:
- 3, calcio: Aunque el compuesto muestra Ca₂, lo que indicaría dos átomos de calcio por cada fórmula unitaria de Ca₂ (PO₄)2, el coeficiente global de 3 multiplica toda la fórmula, incluyendo el calcio. Esto significa que el número total de átomos de calcio es 2 (Ca) * 3 = 6, no 3. La confusión podría surgir al no aplicar el coeficiente a todos los elementos del compuesto.
- 8, oxígeno: Cada grupo PO₄ contiene 4 átomos de oxígeno. Como hay dos grupos de PO₄ en la fórmula y además un coeficiente global de 3, el total de átomos de oxígeno se calcula como 4 (O en PO₄) * 2 (PO₄) * 3 = 24, no 8. La confusión aquí podría ser no multiplicar correctamente por todos los subíndices y el coeficiente global.
Fundamentos generales: Estequiometría
9. ¿Cuántos moles de CO₂ se obtienen a partir de la combustión de 3 mol de C3H8?
Considere la siguiente ecuación C₃H₈+50₂→3CO₂+4H₂O.
- 3 mol
- 6 mol
- 9 mol
Explicación:
Respuesta correcta a c) 9 mol.
Según la ecuación balanceada C₃H₈+5O₂→3CO₂+4H₂O, la relación molar entre el propano (C₃H₈) y el dióxido de carbono (CO₂) es de 1:3. Esto significa que por cada mol de C₃H₈ que se combustiona, se producen 3 moles de CO₂. Al quemar 3 moles de C₃H₈, esta relación se multiplica por 3, resultando en 3×3=9 moles de CO₂.
- a) 3 mol no es correcta porque subestima la cantidad de CO₂ producido. Esta respuesta sugiere incorrectamente que la relación molar entre C₃H₈ y CO₂ es de 1:1, lo cual no coincide con la ecuación balanceada.
- b) 6 mol tampoco es correcta ya que representa el doble de la cantidad de C₃H₈ utilizada pero no considera la relación molar correcta de 1:3. Al aplicar la relación correctamente, es evidente que la cantidad de CO₂ producida es mayor que 6 moles cuando se queman 3 moles de C₃H₈.
Al analizar la ecuación balanceada y entender la relación molar entre los reactivos y los productos, es claro por qué 9 moles es la respuesta correcta y las otras opciones no lo son.
10. Calcule los gramos de AI₂O₃ que se obtienen si se descomponen 2 mol de AI₂ (CO₃)₃ en la siguiente ecuación AI₂ (CO₃)₃→AI2O₃+3CO₂.
Considere:
∙ AI₂ (CO₃)₃=234 g/mol
∙ AI₂O₃=102 g/mol
- 102 g
- 204 g
- 468 g
Explicación:
Respuesta correcta a b) 204 g.
En la descomposición de Al₂(CO₃)₃ para formar Al₂O₃, la relación molar entre Al₂(CO₃)₃ y Al₂O₃ es de 1:1 según la ecuación balanceada Al₂(CO₃)₃ → Al₂O₃ + 3CO₂. Para convertir 2 moles de Al₂O₃ a gramos, utilizamos la masa molar de Al₂O₃ (102 g/mol) multiplicando 2 moles de Al₂O₃ por 102 g/mol, lo que nos da 204 g de Al₂O₃.
- a) 102 g no es correcta porque representa la masa de solo 1 mol de Al₂O₃. Esta respuesta no considera que se están descomponiendo 2 moles de Al₂(CO₃)₃, lo cual, según la relación molar 1:1, resultaría en 2 moles de Al₂O₃.
- c) 468 g también es incorrecta porque no corresponde a la cantidad producida según la relación molar y la masa molar dada. Este número parece ser un cálculo erróneo sin relación directa con la cantidad de moles de Al₂O₃ que se producen en la reacción.
Al seguir la relación molar correcta y aplicar la masa molar adecuadamente, se puede determinar que 204 g es la cantidad correcta de Al₂O₃ producida a partir de la descomposición de 2 moles de Al₂(CO₃)₃.
Fundamentos generales: Reacciones químicas
11. Identifique el tipo de reacción que ocurre en la siguiente ecuación química.
H₂SO₄+2KOH→K₂SO₄+2H₂O
- Neutralización
- Redox
- Combustión
Explicación:
Respuesta correcta a) Neutralización.
La reacción entre el ácido sulfúrico (H₂SO₄) y el hidróxido de potasio (KOH) es un ejemplo clásico de neutralización, donde un ácido y una base reaccionan para formar una sal (K₂SO₄) y agua (H₂O). Este tipo de reacciones es característico de la interacción entre ácidos y bases, llevando a la formación de productos que son notablemente menos reactivos que los reactantes iniciales.
Explicación de por qué las otras no son respuestas correctas:
b) Redox: En una reacción redox, esperaríamos ver un cambio en los estados de oxidación de uno o más elementos en la reacción. Sin embargo, en la reacción dada, no hay transferencia de electrones que cambie los estados de oxidación de los elementos implicados. Tanto el azufre en el H2SO4 como el potasio en el KOH mantienen sus estados de oxidación a lo largo de la reacción, indicando que no se trata de una reacción redox.
c) Combustión: Las reacciones de combustión típicamente involucran un combustible (generalmente un hidrocarburo o un compuesto orgánico) y oxígeno, resultando en la producción de dióxido de carbono y agua, liberando energía en el proceso. La reacción presentada no incluye oxígeno como reactivo en forma libre ni produce energía de la manera característica de las combustiones, y los productos no son los típicos de una reacción de combustión. Por lo tanto, no se clasifica como tal.
12. ¿Cuál es el valor de la entalpía de la siguiente reacción de combustión?
CH₄(g) + 2O₂→ CO₂(g) + 2H₂O(l)
Considere los datos de entalpía parciales.
- ΔHf0(O₂) = 0 kJ/mol
- ΔHf0(CH₄(g)) = -74.81 kJ/mol
- ΔHf0(H2O(l)) = -285.8 kJ/mol
- ΔHf0(CO₂ (g)) = -393.5 kJ/mol
- -890.29 kJ/mol
- -604.49 kJ/mol
- 890.29 kJ/mol
Explicación:

13. Identifique el ejemplo que implica un proceso exotérmico.
- Galvanizar un metal
- Evaporar agua
- Bajar la fiebre
Explicación:
Respuesta correcta a) Bajar la fiebre.
Bajar la fiebre implica un proceso exotérmico en el contexto biológico, donde el cuerpo libera calor hacia el ambiente para reducir la temperatura corporal. Este proceso de disipación de calor es fundamental para restablecer la temperatura normal del cuerpo y es un ejemplo claro de un fenómeno exotérmico, donde se observa el flujo de calor del sistema (el cuerpo) hacia su entorno.
Explicación de por qué las otras no son respuestas correctas:
- Galvanizar un metal: Este proceso implica recubrir un metal con otro para protegerlo contra la corrosión, generalmente mediante un proceso electroquímico. Aunque involucra reacciones químicas, galvanizar un metal en sí mismo no se considera un ejemplo representativo de un proceso exotérmico en el contexto común de entender fenómenos que liberan calor de manera que se perciba como el principal efecto observado.
- Evaporar agua: La evaporación del agua es un proceso endotérmico, no exotérmico. Requiere que el agua absorba calor del ambiente para cambiar de estado líquido a gaseoso. Por lo tanto, en lugar de liberar calor, la evaporación consume energía térmica, lo cual es lo opuesto a lo que caracteriza a un proceso exotérmico.
14. Calcule la constante de equilibrio de la ecuación 3O2 ⇆ 2O3.
Considere los valores:
[O2] = 3 M
[O3] = 3 M
- 0.59 M-1
- 1.33 M-1
- 1.68 M-1
Explicación:


Química orgánica: Átomo de carbono
15. Propiedad del carbono de combinar dos orbitales atómicos puros para formar un nuevo orbital molecular con características propias.
- Isomería
- Hibridación
- Insaturación
Explicación:
Respuesta correcta a: Hibridación.
La hibridación es el proceso mediante el cual dos orbitales atómicos del carbono, como un orbital s y un orbital p, se combinan para formar nuevos orbitales híbridos. Este fenómeno explica cómo el carbono puede establecer varios tipos de enlaces y geometrías moleculares, dependiendo de la estructura específica del compuesto en cuestión. La hibridación es esencial para entender la forma en que los átomos de carbono se unen entre sí y con otros átomos en las moléculas orgánicas.
Razón por la cual las otras opciones no son correctas:
- Isomería: Aunque es una propiedad importante del carbono y sus compuestos, la isomería se refiere a la existencia de dos o más compuestos que tienen la misma fórmula molecular pero estructuras diferentes. No está directamente relacionada con la combinación de orbitales atómicos para formar orbitales moleculares.
- Insaturación: Esta propiedad indica la presencia de enlaces dobles o triples en una molécula, lo que reduce el número de hidrógenos que pueden unirse al carbono. Si bien la insaturación afecta la estructura y reactividad de los compuestos orgánicos, no describe el proceso de combinación de orbitales atómicos para generar nuevos orbitales moleculares.
16. De acuerdo con la estructura, la hibridación del carbono 1 es ___, mientras que la del marcado con el número 3 es ___.
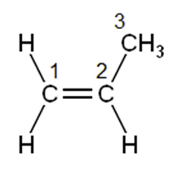
- sp – sp2
- sp2 – sp3
- sp3 – sp
Explicación:
Respuesta correcta b) sp2 – sp3.
El carbono 1, que está unido a dos hidrógenos mediante enlaces simples y a otro carbono mediante un enlace doble, presenta una hibridación sp2. Esto se debe a que la geometría alrededor de este carbono es trigonal plana, típica de la hibridación sp2. Por otro lado, el carbono 3, que forma parte de una molécula de metano, está unido a cuatro hidrógenos mediante enlaces simples, lo que indica una hibridación sp3. Esta hibridación conduce a una geometría tetraédrica, característica de los carbonos unidos a cuatro grupos distintos.
Razón por la cual las otras opciones no son correctas:
- sp – sp2: Esta combinación no es correcta porque un carbono en hibridación sp se encontraría en moléculas con enlaces triples o en estructuras lineales, lo cual no se aplica al carbono 1 descrito. Además, no se ajusta al carbono 3, que es parte de un metano y por ende debe ser sp3.
- sp3 – sp: Esta respuesta es incorrecta porque sugiere que el carbono 1, que tiene un enlace doble, sería sp3, lo cual no coincide con la descripción dada. El enlace doble indica claramente una hibridación sp2. Además, implica incorrectamente que el carbono 3, en el metano, sería sp, cuando en realidad su vinculación a cuatro hidrógenos mediante enlaces simples demuestra una hibridación sp3.
Química orgánica: Estructura y nomenclatura de hidrocarburos
17. Identifique la estructura que representa el 2-penteno.
- H3C − CH2 − CH2 − CH2 − CH3
- H3C − CH = CH − CH2 − CH3
- H3C − C ≡ C − CH2 − CH3
Explicación:
Respuesta correcta b) H3C − CH = CH − CH2 − CH3.
El nombre 2-penteno indica que estamos hablando de un alqueno (indicado por el sufijo “-eno”), con un total de cinco átomos de carbono (indicado por el prefijo “pent-“) y un doble enlace comenzando en el segundo átomo de carbono (indicado por el “2-” delante de “penteno”). La estructura H3C − CH = CH − CH2 − CH3 cumple con todas estas condiciones, con el doble enlace posicionado entre los carbonos 2 y 3.
- La opción a) H3C − CH2 − CH2 − CH2 − CH3 no es correcta porque representa un alcano, específicamente el pentano, y no un alqueno. En esta estructura, todos los enlaces entre los átomos de carbono son sencillos, lo que indica la ausencia de un doble enlace, necesario para conformar un alqueno.
- La opción c) H3C − C ≡ C − CH2 − CH3 tampoco es correcta, ya que muestra un triple enlace entre los carbonos, lo que indica que la molécula es un alquino, específicamente el 2-pentino, no el 2-penteno. En los alquinos, los átomos de carbono conectados por un triple enlace están hibridados sp, mientras que en los alquenos (como el 2-penteno), los átomos de carbono del doble enlace están hibridados sp2.
18. Identifique la geometría del carbono señalado en la estructura.
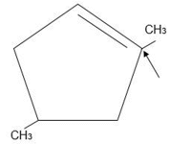
- Trigonal plana
- Tetraédrica
- Lineal
Explicación:
Respuesta correcta a) Trigonal plana.
El carbono señalado en la estructura es parte de un doble enlace, como se puede identificar por la representación de un enlace adicional hacia el carbono adyacente. Esto implica que dicho carbono está hibridado sp2 y los átomos alrededor de este carbono están dispuestos en un plano con ángulos de aproximadamente 120° entre ellos, resultando en una geometría trigonal plana.
- La opción b) Tetraédrica no es correcta porque esta geometría se asocia con carbonos que tienen hibridación sp3, lo que ocurre cuando un átomo de carbono está unido a cuatro sustituyentes mediante enlaces sencillos. En esta estructura, el carbono señalado no tiene cuatro enlaces sencillos, sino un doble enlace y dos enlaces sencillos.
- La opción c) Lineal también es incorrecta para el carbono señalado en la estructura. La geometría lineal se presenta en carbonos con hibridación sp, típicamente encontrados en alquinos, donde el carbono está unido a otros dos átomos a través de un triple enlace o dos dobles enlaces. En este caso, solo hay un doble enlace y, por lo tanto, no corresponde a una geometría lineal.
19. Identifique el nombre IUPAC de la siguiente estructura.
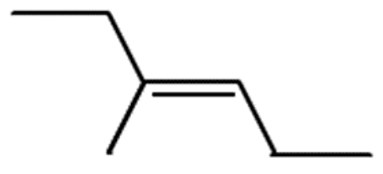
- 2-etil-2-penteno
- 3-metil-3-hexeno
- 4-metil-3-hexeno
Explicación:
Respuesta correcta c) 4-metil-3-hexeno.
Para nombrar la estructura orgánica de acuerdo con las reglas de nomenclatura IUPAC, comenzamos identificando la cadena principal. La cadena principal será la más larga que contenga el doble enlace, para garantizar que este obtenga los localizadores más bajos posibles. En este caso, la cadena más larga contiene seis átomos de carbono, lo que nos da la base hex- para el nombre.
El siguiente paso es identificar la posición del doble enlace. Comenzamos a numerar la cadena principal desde el extremo que nos da los números más bajos a los enlaces múltiples y a los sustituyentes. En la estructura proporcionada, comenzamos a numerar desde el extremo derecho porque al hacerlo, el doble enlace cae en el tercer carbono, que es más bajo que si comenzáramos a numerar desde la izquierda.
Con la cadena principal numerada, identificamos la posición del doble enlace y cualquier sustituyente. Hay un doble enlace que comienza en el carbono número 3 y un grupo metilo (CH₃) en el carbono número 4. Esto nos da la parte del nombre “3-hexeno” para el doble enlace y “4-metil” para el sustituyente.
Juntando todas las partes, el nombre completo para la estructura es 4-metil-3-hexeno.
La numeración comienza desde la derecha para asegurar que el doble enlace tenga el localizador más bajo posible. El doble enlace comienza en el tercer carbono, y hay un grupo metilo en el cuarto carbono, resultando en el nombre 4-metil-3-hexeno según las reglas IUPAC.
Química orgánica: Estructura y nomenclatura de grupos funcionales
20. Identifique el compuesto relacionado con el grupo funcional éster.
- Acetileno
- Acetona
- Propanoato de etilo
Explicación:
Respuesta correcta a c) Propanoato de etilo.
El propanoato de etilo se caracteriza por la presencia del grupo funcional éster, que se identifica por tener un oxígeno enlazado a un carbono por un doble enlace (carbonilo) y a otro oxígeno por un enlace sencillo, este último conectado a su vez a una cadena alquilo. La estructura general de un éster es RCOOR’, donde R y R’ pueden ser cadenas alquílicas o arílicas, pero no necesariamente iguales.
Las razones por las cuales las otras opciones no son correctas son las siguientes:
- Acetileno: El acetileno (o etino) es un hidrocarburo alquino caracterizado por un triple enlace entre dos átomos de carbono (C≡C). No contiene el grupo funcional éster, que implica la presencia de un grupo carbonilo unido a un grupo alquilo o arilo mediante un átomo de oxígeno.
- Acetona: La acetona es el compuesto más sencillo de la clase de las cetonas. Su estructura contiene un grupo carbonilo (C=O) flanqueado por dos grupos metilo (CH3), configurando una estructura propanona (CH3COCH3). Aunque la acetona tiene un grupo carbonilo, no se clasifica como éster porque le falta el grupo alquoxi (OR’) conectado directamente al carbono del grupo carbonilo.
21. ¿Cuál es el nombre del grupo funcional remarcado en el compuesto?
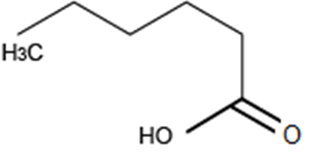
- Cetona
- Ácido carboxílico
- Éter
Explicación:
Respuesta correcta b) Ácido carboxílico.
El grupo funcional remarcado en la estructura es un grupo carboxilo (-COOH), que es característico de los ácidos carboxílicos. Se identifica por tener un átomo de carbono doblemente enlazado a un oxígeno (carbonilo) y un enlace sencillo con un grupo hidroxilo (-OH).
Las otras opciones no son respuestas correctas por las siguientes razones:
a) Cetona: Las cetonas tienen el grupo carbonilo (C=O) conectado a dos radicales de carbono y no presentan un grupo hidroxilo unido directamente al carbono del grupo carbonilo, como se muestra en la estructura.
c) Éter: Los éteres tienen un átomo de oxígeno enlazando dos radicales de carbono. No presentan un grupo carbonilo ni un grupo hidroxilo como parte de su estructura funcional.
22. Identifique la nomenclatura IUPAC del compuesto representado en la estructura.
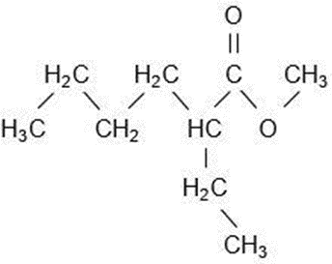
- 2-etilhexanoato de metilo
- Hexanoato de 2-etil-1-metilo
- Metanoato de (2-etil)pentanoilo
Explicación:
Respuesta correcta a) 2-etilhexanoato de metilo.
La nomenclatura IUPAC para ésteres se forma a partir del ácido carboxílico y el alcohol de los cuales derivan. En este caso, la cadena más larga que contiene el grupo funcional carboxilo tiene seis carbonos (hexano), y hay un sustituyente etilo en el carbono número 2. El nombre del grupo alquilo que proviene del alcohol es metilo, indicando que este éster deriva de metanol. Por tanto, el nombre completo del éster es 2-etilhexanoato de metilo, indicando que el grupo metilo está unido al oxígeno del éster.
Las otras opciones no son correctas por las siguientes razones:
b) Hexanoato de 2-etil-1-metilo: Esta opción mezcla incorrectamente la nomenclatura del éster con la de un ácido. El nombre sugiere que hay un grupo metilo directamente unido al grupo carboxílico, lo cual no es consistente con la estructura de un éster.
c) Metanoato de (2-etil)pentanoilo: Esta nomenclatura sugiere que la cadena principal del ácido es metano (un solo carbono), lo cual no es correcto ya que la cadena tiene seis carbonos. Además, el prefijo “(2-etil)pentanoilo” es incorrecto ya que implica una cadena principal de cinco carbonos con un sustituyente etilo, lo cual no concuerda con la estructura proporcionada.
Química orgánica: Enlaces glucosídico y peptídico en las biomoléculas
23. Identifique la estructura que corresponde a un aminoácido.
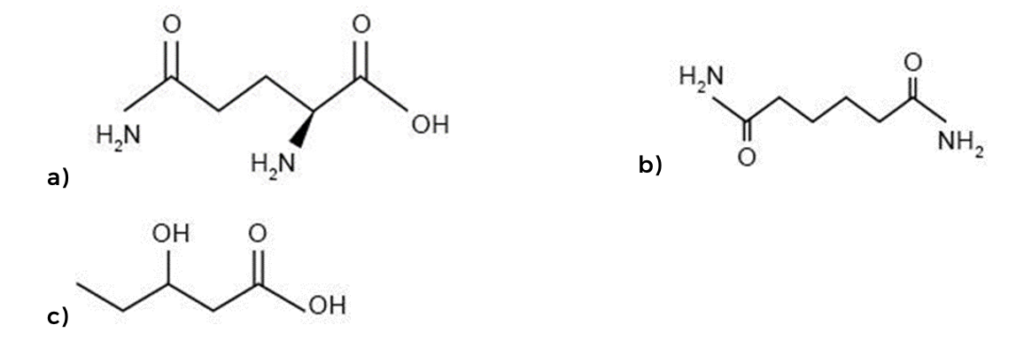
Explicación:
Respuesta correcta a la opción a) La imagen muestra una estructura con un grupo amino en un extremo y un grupo carboxilo en el otro, que son característicos de un aminoácido.
Explicación: Un aminoácido típico está compuesto por un carbono central al cual están unidos un grupo amino (NH2), un grupo carboxilo (COOH), un hidrógeno y un grupo R variable. La estructura de la opción a) muestra estos componentes, identificándola como un aminoácido.
24. Identifique el tipo de enlace que se forma entre los monómeros de la siguiente molécula.

- Glicosídico
- Glucosídico
- Peptídico
Explicación:
Respuesta correcta a la opción a) Glicosídico.
La estructura muestra varios anillos de carbono con grupos hidroxilo (–OH) y un grupo metoxi (–OCH3), lo que indica que es probable que sea un tipo de carbohidrato complejo o un glucósido. Los enlaces glicosídicos se forman típicamente entre los grupos OH de monosacáridos y pueden involucrar la unión a otros grupos como –OH, –NH2 o –SH. Por lo tanto, la molécula parece contener enlaces glicosídicos.
Por qué las otras opciones no son correctas:
- La opción b) Glucosídico no es la más precisa en el contexto de la pregunta. Aunque el término “glucosídico” puede usarse para describir enlaces en glucósidos específicamente derivados de la glucosa, el término “glicosídico” es más general y se refiere a cualquier enlace que une un azúcar (monosacárido) en un glucósido, por lo que es más apropiado para la descripción general de enlaces en carbohidratos.
- La opción c) Peptídico no es correcta porque los enlaces peptídicos se forman entre aminoácidos en las proteínas, y la estructura no muestra los grupos amino (–NH2) ni carboxilo (–COOH) que definirían los aminoácidos ni un enlace peptídico.
Recomendaciones finales
Para sacar el máximo provecho de este simulador:
- Estudia con tiempo limitado para simular la presión real del examen.
- Revisa tus errores y comprende la lógica detrás de cada respuesta.
- Refuerza los temas en los que tengas más fallos hasta dominarlos.
- Realiza simulacros completos para entrenar tu resistencia mental.
- No te quedes solo con la práctica básica: en Pasatuexam encontrarás guías detalladas, ejemplos paso a paso y explicaciones extendidas que harán tu preparación más sencilla.
- Empieza gratis con los temas liberados, pero si quieres cubrir todo el temario y llegar con ventaja, desbloquea el curso completo.
Con Pasatuexam tendrás un plan estructurado, reactivos reales y explicaciones claras que te acercarán a tu lugar en la universidad de tus sueños.
🚀 ¡Potencia tu Preparación con Nuestro Plan Profesional! 🎓
Si has empezado a descubrir cómo prepararte para el EXANI-II con nuestro contenido gratuito, ¡te felicitamos! 🌟 Pero, ¿estás listo para dar el gran salto? Con nuestro Plan Profesional, no solo vas un paso adelante, ¡vas a volar! 🚀
Al elegir el Plan Profesional, desbloquearás acceso a:
- Contenido sin Publicidad y sin Interrupciones 🚫: Estudia con la máxima concentración, sin anuncios que te distraigan de tus objetivos.
- Contenido de Calidad 100% Basado en las Guías del EXANI-II 📚: Confía en un material que sigue fielmente el currículo oficial, maximizando tu eficacia en el estudio.
- Lecciones Escritas y Videos Explicativos 📝🎥: Visualiza conceptos complejos con materiales diseñados para facilitar tu aprendizaje.
- Explicaciones Paso a Paso 📘: Todo se entiende mejor con nuestros métodos sencillos y claros.
- Preguntas Como en el Examen ❓: Practica con ejercicios que te preparan de verdad, aumentando tu seguridad al máximo.
- Simuladores de Examen 💻: Siente el día del examen antes de llegar, para que nada te sorprenda.
- Acceso Multiplataforma 📱💻: Aprende cuando quieras y desde cualquier dispositivo, facilitando tu preparación en todo momento.
Asegura tu acceso al éxito con el Plan Profesional. No es solo preparación, es tu boleto para lograr tus sueños universitarios. ¡Decídete ya! 🌈 No dejes pasar esta oportunidad. ⏳ ¡El tiempo vuela y tu futuro te espera!
🌟 Simulador Gratis 🌟
Si estás curioso sobre lo que el Plan Profesional puede ofrecerte, te tenemos una sorpresa. Haz clic aquí y enfrenta nuestro simulador especial. Con solo 30 preguntas, podrás medir qué tan preparado estás para tu examen de admisión. 🎯
Esta es tu oportunidad de obtener un vistazo de la calidad y profundidad que nuestro Plan Profesional tiene para ofrecer, y al mismo tiempo, evaluar tu nivel actual de preparación. 💪

